Соединения углерода
1. Заполните таблицу 7.

2. Опишите физиологическое действие угарного газа на организм человека
Связывает необратимо гемоглобил
Объясните, что является противоядием при отравлении угарным газом
Свежий воздух
3. Запишите не менее двух уравнений реакций, в результате которых образуется:
а) угарный газ б) углекислый газ
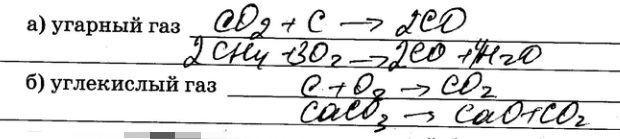
Для двух ОВР составьте электронный баланс, а для реакции обмена ионные уравнения.
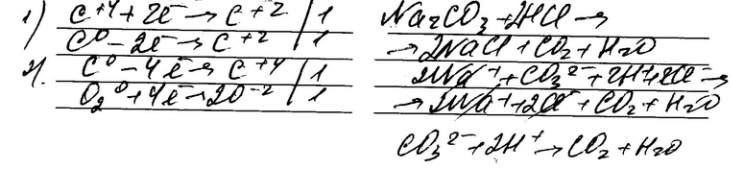
4. Изобразите прибор (рис. 9), в котором можно получить и собрать углекислый газ. Подпишите формулы исходных веществ и продуктов реакции.

Опишите два способа обнаружения выделяющегося углекислого газа?
1) с Ca(OH)2 образует осадок CaCO3
2) CaCO3 + CO2 + H2O -> Ca(HCO3)2 Осадок далее переходит в прозрачный раствор
5. Изготовьте на отдельном листе бумаги формата А4 коллаж «Применение углекислого газа» или «Применение угарного газа» (по выбору). - Самостоятельно
6. Составьте уравнение реакции образования угольной кислоты
1) Na2CO3 + H2SO4 -> Na2SO4 + CO2 + H2O
2) CO2 + H2O <-> H2CO3
Укажите тип записанной реакции:
1) По числу и составу исходных веществ и продуктов реакции: соединение
2) По обратимости: обратимая
3) По изменению степеней окисления элементов: не ОВР
4) По использованию катализатора: некаталитическая
7. Дайте характеристику угольной кислоте, вписав пропущенные слова и словосочетания, формулы.
1. Формула H2CO3
2. Тип вещества - Сложное. Класс вещества - Кислота. Характеристика вещества: 1) По наличию кислорода - кислородная; 2) По основности - двухосновная; 3) По растворимости в воде - растворимая; 4) По степени электролитической диссоциации - слабая; 5) По стабильности - нестабильная.
3. Физические свойства - Очень нестойкая кислота, легко разлагается с образованием CO2 и H2O
4. Химические свойства - Взаимодействует с карбонатами, щелочами
5. Применение - Применяется для получения карбонатов, гидрокарбонатов, "дым" на сцене, тушения пожаров.
8. Заполните схему 10 формулами и названиями соединений.
Карбонаты: Na2CO3 - карбонат натрия; BaCO3 - карбонат бария
Гидрокарбонаты: NaHCO3 - гидрокарбонат натрия; Ca(HCO3)2 - гидрокарбонат кальция
9. Составьте уравнения реакций соответствующие схеме:
CO2 -> CaCO3 <-> Ca(HCO3)2 -> CO2
1) CO2 + CaO -> CaCO3
2) CaCO3 + CO2 + H2O -> Ca(HCO3)2
3) Ca(HCO3)2 ->(t) CaCO3 + CO2 + H2O
Объясните, где в природе происходят превращения, уравнения реакций которых вы составили.
1) Растворение солей Ca в H2O
2) Образование сталактитов и сталагмитов
10. Составьте опорный конспект "Жесткость воды" - Самостоятельно